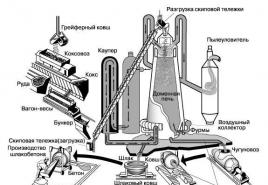
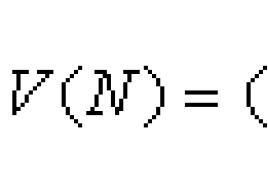kimerült uránium. Az uránmag hasadása. Láncreakció. A folyamat leírása Az urán 238 hasadása
A radioaktivitás jelenségének tanulmányozása során minden tudós olyan fontos jellemzőre hivatkozik, mint a felezési ideje. Mint tudják, azt mondja, hogy a világon minden másodpercben atomok bomlanak, miközben ezeknek a folyamatoknak a mennyiségi jellemzői közvetlenül összefüggenek a jelenlévő atomok számával. Ha egy bizonyos időn belül a rendelkezésre álló atomok teljes számának fele elbomlik, akkor a fennmaradó atomok ½ bomlásához ugyanennyi idő kell. Ezt az időszakot nevezzük felezési időnek. Különböző elemek esetében ez eltérő - ezredmásodperctől több milliárd évig, mint például az urán felezési idejének esetében.
Az urán, mint a Földön természetesen létező összes elem közül a legnehezebb, általában a legkiválóbb tárgy a radioaktivitás folyamatának tanulmányozására. Ezt az elemet még 1789-ben fedezte fel M. Klaproth német tudós, aki a nemrég felfedezett Uránusz bolygó tiszteletére nevezte el. Azt a tényt, hogy az urán radioaktív, egészen véletlenül állapította meg a 19. század végén A. Becquerel francia kémikus.
Az Uránusz kiszámítása ugyanazzal a képlettel történik, mint más radioaktív elemek analóg periódusai:
T_(1/2) = au ln 2 = frac(ln 2) (lambda),
ahol az "au" az atom átlagos élettartama, a "lambda" a fő bomlási állandó. Mivel az ln 2 körülbelül 0,7, a felezési idő átlagosan csak 30%-kal rövidebb, mint egy atom teljes élettartama.
Annak ellenére, hogy ma a tudósok az urán 14 izotópját ismerik, ezek közül csak három fordul elő a természetben: urán-234, urán-235 és urán-238. az urán más: tehát az U-234 esetében "csak" 270 ezer év, az urán-238 felezési ideje pedig meghaladja a 4,5 milliárdot. Az urán-235 felezési ideje az "arany középút" - 710 millió év.
Meg kell jegyezni, hogy az urán radioaktivitása természetes körülmények között meglehetősen magas, és lehetővé teszi például a fényképészeti lemezek megvilágítását mindössze egy órán keresztül. Ugyanakkor érdemes megjegyezni, hogy az összes uránizotóp közül csak az U-235 alkalmas urán töltelék készítésére, itt minimális.
Az urán-238 felezési ideje jóval több, mint 4 milliárd év, de ma már aktívan használják a nukleáris iparban. Tehát ahhoz, hogy láncreakciót indítsunk el ennek az elemnek a nehéz atommagjainak hasadásához, jelentős mennyiségű neutronenergiára van szükség. Az urán-238-at hasadási és fúziós berendezésekben védelemként használják. A bányászott urán-238 nagy részét azonban plutónium szintetizálására használják, amelyet nukleáris fegyverekben használnak.
A tudósok az urán felezési idejét használják az egyes ásványok és égitestek életkorának kiszámításához. Az uránóra meglehetősen univerzális mechanizmus az ilyen számításokhoz. Ugyanakkor a kor többé-kevésbé pontos kiszámításához nemcsak az urán mennyiségét kell ismerni bizonyos kőzetekben, hanem az urán és az ólom, mint végtermék, amelyvé az uránmagok alakulnak, arányát is ismerni kell.
A kőzetek és ásványok kiszámításának van egy másik módja is, ez az úgynevezett spontánhoz kapcsolódik.Mint ismeretes, az urán természetes körülmények között történő spontán hasadása következtében részecskéi kolosszális erővel bombázzák a közeli anyagokat, különleges nyomokat hagyva maguk után - számokat.
E nyomok számából, egyúttal az urán felezési idejének ismeretében vonnak le következtetést a tudósok egy adott szilárd test korára - legyen az egy ősi szikla vagy egy viszonylag „fiatal” váza. A helyzet az, hogy egy objektum életkora egyenesen arányos az uránatomok mennyiségi indexével, amelyek atommagjai bombázták.
A cikk tartalma
URÁNUSZ, U (urán), az aktinidák családjába tartozó fémes kémiai elem, amely magában foglalja az Ac, Th, Pa, U és a transzurán elemeket (Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr) ). Az urán nukleáris fegyverekben és atomenergiában való felhasználásáról vált híressé. Az urán-oxidokat üveg és kerámia színezésére is használják.
Megtalálás a természetben.
A földkéreg urántartalma 0,003%, a föld felszíni rétegében négyféle lerakódás formájában fordul elő. Először is, ezek uraninit vagy uránszurok (urán-dioxid UO 2) erek, amelyek uránban nagyon gazdagok, de ritkák. Rádiumlerakódások kísérik őket, mivel a rádium az urán izotópos bomlásának közvetlen terméke. Ilyen erek találhatók Zaire-ben, Kanadában (Nagy Medve-tó), Csehországban és Franciaországban. A második uránforrás a tórium és az uránérc konglomerátumai, valamint más fontos ásványok ércek. A konglomerátumok általában elegendő mennyiségű aranyat és ezüstöt tartalmaznak a kinyeréshez, és az urán és a tórium kísérőelemekké válnak. Ezen ércek nagy lelőhelyei Kanadában, Dél-Afrikában, Oroszországban és Ausztráliában találhatók. A harmadik uránforrás a karnotitban (kálium-uranil-vanadát) gazdag üledékes kőzetek és homokkövek, amelyek az uránon kívül jelentős mennyiségű vanádiumot és egyéb elemeket is tartalmaznak. Ilyen ércek az Egyesült Államok nyugati államaiban találhatók. A vas-urán palák és foszfátércek jelentik a negyedik lerakódási forrást. Gazdag lelőhelyek találhatók Svédország palában. Néhány foszfátérc Marokkóban és az Egyesült Államokban jelentős mennyiségű uránt tartalmaz, az angolai és a közép-afrikai köztársasági foszfátlelőhelyek pedig még gazdagabbak uránban. A legtöbb lignit és néhány szén általában uránszennyeződést tartalmaz. Uránban gazdag lignit lelőhelyeket találtak Észak- és Dél-Dakotában (USA), bitumenes szenet pedig Spanyolországban és Csehországban.
Nyítás.
Az uránt 1789-ben fedezte fel M. Klaproth német kémikus, aki az Uránusz bolygó nyolc évvel korábbi felfedezésének tiszteletére nevezte el az elemet. (Klaproth korának vezető kémikusa volt; más elemeket is felfedezett, köztük a Ce-t, Tit-t és Zr-t.) Valójában a Klaproth által nyert anyag nem elemi urán volt, hanem annak oxidált formája, és az elemi urán volt az első E. .Peligot francia vegyész szerezte meg 1841-ben. A felfedezés pillanatától egészen a XX. Az urán nem volt olyan fontos, mint manapság, bár számos fizikai tulajdonságát, valamint az atomtömeget és -sűrűséget meghatározták. 1896-ban A. Becquerel megállapította, hogy az uránsók olyan sugárzással rendelkeznek, amely megvilágítja a fényképezőlapot a sötétben. Ez a felfedezés ösztönözte a vegyészeket a radioaktivitás kutatására, 1898-ban pedig a francia fizikusok, házastársak, P. Curie és M. Sklodowska-Curie a radioaktív elemek polónium és rádium sóit, valamint E. Rutherford, F. Soddy, C. Faience és más tudósok kidolgozták a radioaktív bomlás elméletét, amely lefektette a modern nukleáris kémia és nukleáris energia alapjait.
Az urán első alkalmazásai.
Bár az uránsók radioaktivitása ismert volt, érceit e század első harmadában csak a vele járó rádium előállítására használták, és az uránt nemkívánatos mellékterméknek tartották. Felhasználása elsősorban a kerámiatechnológiában és a kohászatban összpontosult; Az urán-oxidokat széles körben használták az üveg színezésére halványsárgától sötétzöldig, ami hozzájárult az olcsó üveggyártás fejlődéséhez. Ma az ezen iparágak termékeit ultraibolya fényben fluoreszkálóként azonosítják. Az első világháború idején és röviddel azután az uránt keményfém formájában a Mo-hoz és a W-hoz hasonlóan szerszámacélok gyártására is használták; 4–8%-os uránium váltotta fel az akkoriban korlátozott termelésű volfrámot. A szerszámacélok előállításához 1914–1926-ban évente több tonna ferrouránt állítottak elő, amely legfeljebb 30 tömeg% U-t tartalmazott. Az urán ezen felhasználása azonban nem tartott sokáig.
Az urán modern felhasználása.
Az uránipar 1939-ben kezdett formát ölteni, amikor a 235 U uránizotóp hasadását hajtották végre, ami az uránhasadás szabályozott láncreakcióinak műszaki megvalósításához vezetett 1942 decemberében. Ekkor született meg az atom korszaka, amikor az urán kisebb elemből az élettársadalom egyik legfontosabb elemévé vált. Az urán katonai jelentősége az atombomba előállításában és az atomreaktorokban való üzemanyagként való felhasználása csillagászatilag megnövekedett uránigényt teremtett. Az urán iránti kereslet növekedésének érdekes kronológiája a Great Bear Lake (Kanada) lelőhelyeinek történetén alapul. 1930-ban ebben a tóban fedezték fel a gyanta keveréket, az urán-oxidok keverékét, 1932-ben pedig a rádium tisztítására szolgáló technológiát alakították ki ezen a területen. Minden tonna ércből (kátránykeverék) 1 g rádiumot és körülbelül fél tonna mellékterméket - uránkoncentrátumot - kaptak. A rádium azonban kevés volt, kitermelését leállították. 1940 és 1942 között a fejlesztés újraindult, és uránércet szállítottak az Egyesült Államokba. 1949-ben az urán hasonló tisztítását, némi módosítással, tiszta UO 2 előállítására alkalmazták. Ez a termelés nőtt, és mára az egyik legnagyobb urántermelés.
Tulajdonságok.
Az urán az egyik legnehezebb elem a természetben. A tiszta fém nagyon sűrű, képlékeny, elektropozitív, alacsony elektromos vezetőképességgel és nagyon reaktív.
Az uránnak három allotróp módosulata van: a-urán (ortorombikus kristályrács), szobahőmérséklettől 668 ° C-ig terjedő tartományban létezik; b- urán (egy tetragonális típusú összetett kristályrács), stabil a 668–774 ° С tartományban; g- urán (testközpontú köbös kristályrács), 774 °C-tól olvadáspontig (1132 °C) stabil. Mivel az urán minden izotópja instabil, minden vegyülete radioaktivitást mutat.
Az urán izotópjai
238 U, 235 U, 234 U 99,3:0,7:0,0058 arányban találhatók meg a természetben, nyomokban pedig 236 U. Az összes többi uránizotóp 226 U-tól 242 U-ig mesterségesen nyerhető. A 235 U izotóp különösen fontos. Lassú (termikus) neutronok hatására hatalmas energia felszabadulásával osztódik. 235 U teljes hasadása 2h 10 7 kWh/kg "hőenergia-egyenérték" felszabadulását eredményezi. A 235 U hasadása nemcsak nagy mennyiségű energia előállítására használható, hanem más fontos aktinid elemek szintetizálására is. A természetes izotóp uránt atomreaktorokban lehet felhasználni 235 U hasadással előállított neutronok előállítására, míg a láncreakcióhoz nem szükséges neutronfelesleget egy másik természetes izotóp fogja be, ami plutóniumtermelést eredményez:
Amikor gyors neutronok 238 U-vel bombázzák, a következő reakciók lépnek fel:
E séma szerint a legelterjedtebb 238 U izotóp plutónium-239-é alakítható, amely a 235 U-hoz hasonlóan szintén képes a lassú neutronok hatására hasadni.
Jelenleg az urán nagyszámú mesterséges izotópját sikerült előállítani. Közülük a 233 U különösen figyelemre méltó, mivel a lassú neutronokkal való kölcsönhatás során is hasad.
Az urán néhány más mesterséges izotópját gyakran használják radioaktív jelölésként (nyomjelzőként) a kémiai és fizikai kutatásokban; ez mindenekelőtt b- emitter 237 U és a- emitter 232 U.
Kapcsolatok.
Az urán, egy nagyon reaktív fém, oxidációs állapota +3 és +6 között van, az aktivitási sorozatban közel áll a berilliumhoz, kölcsönhatásba lép minden nemfémmel és intermetallikus vegyületeket képez Al, Be, Bi, Co, Cu, Fe, Hg , Mg, Ni, Pb, Sn és Zn. A finom eloszlású urán különösen reaktív, és 500 °C feletti hőmérsékleten gyakran az urán-hidridre jellemző reakciókba lép. A csomós urán vagy forgács 700-1000°C-on fényesen ég, míg az urángőzök már 150-250°C-on égnek; az urán 200-400°C-on reagál a HF-el, UF 4 és H 2 képződve. Az urán tömény HF-ben vagy H 2 SO 4-ben és 85% H 3 PO 4-ben lassan oldódik még 90 °C-on is, de könnyen reagál tömény hidrogénnel. HCl és kevésbé aktív HBr vagy HI esetén. Az urán reakciója híg és tömény HNO 3-mal a legaktívabban és leggyorsabban az uranil-nitrát képződésével megy végbe ( lásd lejjebb). HCl jelenlétében az urán gyorsan oldódik szerves savakban, és U 4+ szerves sókat képez. Az urán az oxidáció mértékétől függően többféle sót képez (közülük a legfontosabb az U 4+, az egyik az UCl 4 egy könnyen oxidálódó zöldsó); Az UO 2 (NO 3) 2 típusú uranil-sók (UO 2 2+ gyök) sárgák és zölden fluoreszkálnak. Az uranil-sók az UO 3 (sárga színű) amfoter-oxid savas közegben való feloldásával keletkeznek. Lúgos környezetben az UO 3 Na 2 UO 4 vagy Na 2 U 2 O 7 típusú uránátokat képez. Ez utóbbi vegyületet ("sárga uranil") porcelánmázak és fluoreszkáló üvegek gyártására használják.
Az urán-halogenideket az 1940-es és 1950-es években széles körben tanulmányozták, mivel ezek képezték az alapját az atombombához vagy atomreaktorhoz szükséges uránizotópok szétválasztásának módszereinek kidolgozásának. Az UF 3 urán-trifluoridot UF 4 hidrogénnel történő redukciójával, az UF 4 urán-tetrafluoridot pedig különféle módokon HF oxidokkal, például UO 3 vagy U 3 O 8 reakciójával vagy uranilvegyületek elektrolitikus redukciójával nyerik. Az UF 6 urán-hexafluoridot U vagy UF 4 elemi fluorral történő fluorozásával vagy oxigén UF 4 -re gyakorolt hatására állítják elő. A hexafluorid 64°C-on (1137 Hgmm) magas törésmutatójú átlátszó kristályokat képez; a vegyület illékony (56,54 °C-on normál nyomáson szublimál). Az urán-oxohalogenidek, például az oxofluoridok összetétele UO 2 F 2 (uranil-fluorid), UOF 2 (urán-oxid-difluorid).
Az urán radioaktív fém. A természetben az urán három izotópból áll: urán-238, urán-235 és urán-234. A legmagasabb stabilitási szintet az urán-238 esetében észlelték.
| Jellegzetes | Jelentése |
|---|---|
| Általános információ | |
| Név, szimbólum | Urán-238, 238U |
| Alternatív címek | urán egy, UI |
| Neutronok | 146 |
| Protonok | 92 |
| Nuklidok tulajdonságai | |
| Atomtömeg | 238.0507882(20) a. eszik. |
| Tömegfelesleg | 47 308,9(19) keV |
| Fajlagos kötési energia (nukleononként) | 7570.120(8) keV |
| Izotóp bőség | 99,2745(106) % |
| Fél élet | 4 468 (3) 109 év |
| Bomlástermékek | 234th, 238Pu |
| Szülői izotópok | 238 Pa (β−) 242Pu(α) |
| Az atommag spinje és paritása | 0+ |
| Bomlási csatorna | Bomlási energia |
| α-bomlás | 4.2697(29) MeV |
| SF | |
| ββ | 1.1442(12) MeV |
az urán radioaktív bomlása
A radioaktív bomlás az atommagok összetételének vagy belső szerkezetének hirtelen megváltozásának folyamata, amelyet instabilitás jellemez. Ebben az esetben elemi részecskék, gamma-kvantumok és/vagy nukleáris fragmentumok bocsátanak ki. A radioaktív anyagok radioaktív magot tartalmaznak. A radioaktív bomlásból származó leánymag is radioaktívvá válhat, és egy bizonyos idő után bomláson megy keresztül. Ez a folyamat addig folytatódik, amíg egy stabil, radioaktivitástól mentes mag nem képződik. E. Rutherford 1899-ben kísérletileg bebizonyította, hogy az uránsók háromféle sugarat bocsátanak ki:
- α-sugarak - pozitív töltésű részecskék áramlása
- β-sugarak - negatív töltésű részecskék áramlása
- γ-sugarak - nem hoznak létre eltéréseket a mágneses térben.
| A sugárzás típusa | Nuklid | Fél élet |
|---|---|---|
| Ο | Uránusz - 238 U | 4,47 milliárd év |
| α ↓ | ||
| Ο | Tórium - 234 Th | 24,1 nap |
| β ↓ | ||
| Ο | Protactinium - 234 Pa | 1,17 perc |
| β ↓ | ||
| Ο | urán - 234 U | 245.000 év |
| α ↓ | ||
| Ο | Tórium - 230 Th | 8000 év |
| α ↓ | ||
| Ο | Rádium - 226 Ra | 1600 év |
| α ↓ | ||
| Ο | Polónium - 218 Po | 3,05 perc |
| α ↓ | ||
| Ο | Ólom - 214 Pb | 26,8 perc |
| β ↓ | ||
| Ο | Bizmut - 214 Bi | 19,7 perc |
| β ↓ | ||
| Ο | Polónium - 214 Po | 0,000161 másodperc |
| α ↓ | ||
| Ο | Ólom - 210 Pb | 22,3 év |
| β ↓ | ||
| Ο | Bizmut - 210 Bi | 5,01 nap |
| β ↓ | ||
| Ο | Polónium - 210 Po | 138,4 nap |
| α ↓ | ||
| Ο | Ólom - 206 Pb | stabil |
Az urán radioaktivitása
A természetes radioaktivitás az, ami megkülönbözteti a radioaktív uránt a többi elemtől. Az uránatomok minden tényezőtől és körülménytől függetlenül fokozatosan változnak. Ebben az esetben láthatatlan sugarakat bocsátanak ki. Az uránatomokkal végbemenő átalakulások után egy másik radioaktív elemet kapunk, és a folyamat megismétlődik. Annyiszor megismétli, ahányszor szükséges, hogy egy nem radioaktív elemet kapjon. Például néhány transzformációs lánc legfeljebb 14 szakaszból áll. Ebben az esetben a köztes elem a rádium, az utolsó szakasz pedig az ólomképződés. Ez a fém nem radioaktív elem, ezért számos átalakulás megszakad. Az urán teljes ólommal történő átalakulása azonban több milliárd évbe telik.
A radioaktív uránérc gyakran okoz mérgezést az urán nyersanyagok kitermelésével és feldolgozásával foglalkozó vállalkozásoknál. Az emberi szervezetben az urán általános sejtméreg. Főleg a vesét érinti, de előfordulnak máj- és gyomor-bélrendszeri elváltozások is.
Az uránnak nincsenek teljesen stabil izotópjai. A leghosszabb élettartamot az urán-238-nak tartják. Az urán-238 félbomlása 4,4 milliárd év alatt megy végbe. Valamivel kevesebb, mint egymilliárd év az urán-235 bomlási ideje – 0,7 milliárd év. Az urán-238 a természetes urán teljes térfogatának több mint 99%-át foglalja el. Kolosszális felezési ideje miatt ennek a fémnek a radioaktivitása nem magas, például az alfa-részecskék nem tudnak áthatolni az emberi bőr stratum corneumán. A tudósok egy sor vizsgálatot követően megállapították, hogy a fő sugárforrás nem maga az urán, hanem az általa képződött radongáz, valamint annak bomlástermékei, amelyek légzés közben kerülnek az emberi szervezetbe.
Uránusz
Az urán, a 92-es elem a természetben található legnehezebb elem. Már korunk elején használták, Pompeii és Herculaneum romjai között sárga mázas (több mint 1% urán-oxidot tartalmazó) kerámiatöredékeket találtak.
Az uránt 1789-ben fedezte fel Marton Heinrich Klaproth német kémikus az uránszurokban, aki az 1781-ben felfedezett urán bolygóról nevezte el. Eugene Peligot francia kémikus először 1841-ben nyert fémuránt vízmentes urán-tetraklorid káliummal való redukálásával. 1896-ban Antoine-Henri Becquerel fedezte fel az urán radioaktivitásának jelenségét azáltal, hogy véletlenül egy közelben lévő uránsódarab ionizáló sugárzását tette ki a fényképező lemezekre.
Kémiai és fizikai tulajdonságok
Az urán egy nagyon nehéz, ezüstös fehér, fényes fém. Tiszta formájában valamivel puhább, mint az acél, alakítható, rugalmas, enyhe paramágneses tulajdonságokkal rendelkezik. Az uránnak három allotróp formája van: alfa (prizmás, 667,7 °C-ig stabil), béta (négyszögletű, 667,7-774,8 °C-on stabil), gamma (testközpontú köbös szerkezetű, 774,8 °C-tól olvadáspontig létezik). ), amelyben az urán a leginkább képlékeny és könnyen feldolgozható. Az alfa fázis egy nagyon figyelemreméltó típusú prizmás szerkezet, amely hullámos atomrétegekből áll egy rendkívül aszimmetrikus prizmás rácsban. Ez az anizotróp szerkezet megnehezíti az urán más fémekkel való ötvözését. Csak a molibdén és a nióbium képezhet szilárd ötvözetet az uránnal. Igaz, a fémes urán számos ötvözettel kölcsönhatásba léphet, intermetallikus vegyületeket képezve.
Az urán alapvető fizikai tulajdonságai:
olvadáspont: 1132,2 °C (+/- 0,8);
forráspontja 3818 °C;
sűrűség 18,95 (alfa fázisban);
fajhő 6,65 cal/mol/°C (25 C);
szakítószilárdság 450 MPa.
Kémiailag az urán nagyon aktív fém. Levegőn gyorsan oxidálódik, irizáló oxidfilm borítja. A finom uránpor levegőben spontán meggyullad, 150-175 °C hőmérsékleten meggyullad, U 3 O 8 képződik. 1000 °C-on az urán nitrogénnel egyesül, így sárga urán-nitrid keletkezik. A víz korrodálhatja a fémet, alacsony hőmérsékleten lassan, magas hőmérsékleten pedig gyorsan. Az urán sósavban, salétromsavban és más savakban oldódik, négy vegyértékű sókat képezve, de nem lép kölcsönhatásba lúgokkal. Az urán kiszorítja a hidrogént a szervetlen savakból és olyan fémek sóoldataiból, mint a higany, ezüst, réz, ón, platina és arany. Erős rázással az urán fémrészecskéi izzani kezdenek.
Az uránnak négy oxidációs állapota van - III-VI. A hat vegyértékű vegyületek közé tartozik az uranil-trioxid UO 3 és az uranil-klorid UO 2 Cl 2. Az urán-tetraklorid UCl 4 és az urán-dioxid UO 2 a négy vegyértékű urán példái. A négy vegyértékű uránt tartalmazó anyagok általában instabilak és hat vegyértékűekké alakulnak, ha hosszú ideig vannak kitéve levegőnek. Az uranil-sók, például az uranil-klorid erős fény vagy szerves anyagok jelenlétében lebomlanak.
Az urán izotópjai
Az uránnak 14 izotópja van, amelyek közül csak három fordul elő a természetben. A természetes urán hozzávetőleges izotóp-összetétele a következő:
Bár az U-235 izotóp tartalma általában állandó, mennyiségében előfordulhat némi ingadozás az érc kimerülése miatt a hasadási reakciók miatt, amelyek akkor mentek végbe, amikor az U-235 koncentrációja jóval magasabb volt a mainál. A leghíresebb ilyen természetes "reaktort", 1,9 milliárd éves, 1972-ben fedezték fel Gabonban az Oklo-bányában. Amikor ez a reaktor működött, a természetes urán 3% U-235-öt tartalmazott, ami annyi, mint a modern atomerőművek üzemanyaga. Mára a bánya magja kiégett és kimerült, mindössze 0,44% U-235-öt tartalmaz. Az oklói és a közelben megnyitott természetes reaktorok az egyetlenek a maguk nemében.
Az érc U-234 tartalma nagyon alacsony. Az U-235-től és az U-238-tól eltérően rövid élettartama miatt ennek az izotópnak a teljes mennyisége az U-238 atomok bomlása következtében képződik:
U 238 -> (4,51 milliárd év, alfa-bomlás) -> Th 234
Th 234 -> (24,1 nap, béta-bomlás) -> Pa 234
Pa 234 -> (6,75 óra, béta-bomlás) -> U 234
Általában az U-234 egyensúlyban van az U-238-cal, ugyanolyan sebességgel bomlik és képződik. A bomló U-238 atomok azonban egy ideig léteznek tórium és protaktinum formájában, így kémiailag vagy fizikailag elválaszthatók az érctől (a talajvíz kioldja őket). Mivel az U-234 felezési ideje viszonylag rövid, az ércben található összes izotóp az elmúlt néhány millió évben keletkezett. A természetes urán radioaktivitásának körülbelül a fele az U-234 hozzájárulása.
Az U-236 felezési ideje 23,9 millió év, és a természetben nem fordul elő jelentős mennyiségben. Felhalmozódik, ha az uránt neutronokkal sugározzák be a reaktorokban, ezért a kiégett urán nukleáris fűtőanyag "jelzéseként" használják.
A természetes urán fajlagos radioaktivitása 0,67 mikrocurie/g (az U-234 és U-238 között csaknem felére oszlik, az U-235 kis mértékben járul hozzá). A természetes urán elég radioaktív ahhoz, hogy körülbelül egy óra alatt megvilágítsa a fényképezőt.
U-235.
A természetes uránban csak egy, viszonylag ritka izotóp alkalmas atombomba magjának elkészítésére vagy egy erőreaktorban végbemenő reakció támogatására. Az U-235 dúsítás mértéke az atomerőművek nukleáris üzemanyagában 2-4,5%, fegyverhasználat esetén - legalább 80%, előnyösebben 90%. Az Egyesült Államokban a fegyveres minőségű urán-235 dúsítása 93,5%, az ipar 97,65% -ot képes előállítani - az ilyen minőségű uránt a haditengerészet reaktoraiban használják.
1998-ban az Oak Ridge National Laboratory (ORNL) izotóposztálya 93%-os U-235-öt szállított 53 USD/g áron.
Mivel még könnyebb, az U-234 arányosan még jobban is dúsult, mint az U-235 minden tömegkülönbségen alapuló elválasztási eljárásban. Az erősen dúsított U-235 jellemzően 1,5-2,0% U-234-et tartalmaz.
Az U-235 spontán hasadásának intenzitása 0,16 osztás/s*kg. A nettó 60 kilogramm tömegű U-235 mindössze 9,6 fiss/s sebességet produkál, így elég könnyű ágyúkört építeni. Az U-238 kilogrammonként 35-ször több neutront hoz létre, így ennek az izotópnak egy kis százaléka is többszörösére emeli ezt a számot. Az U-234 22-szer több neutront termel, és hasonló nemkívánatos hatással bír, mint az U-238.
Az U-235 fajlagos aktivitása mindössze 2,1 mikrocurie/g; 0,8%-os U-234-gyel való szennyeződése 51 mikrocurie/g-ra emeli.
U-238.
Bár az urán-238 nem használható elsődleges hasadóanyagként, a hasadáshoz szükséges neutronok nagy energiája miatt fontos helye van az atomiparban.
Az U-238 nagy sűrűségével és atomtömegével alkalmas töltés/reflektorhéj készítésére belőle fúziós és hasadó eszközökben. Az a tény, hogy gyors neutronokkal hasadó, növeli a töltés energiahozamát: közvetve, a visszavert neutronok megsokszorozásával; közvetlenül a héjmagok gyors neutronok általi hasadása során (szintézis során). A hasadás során keletkező neutronok körülbelül 40%-a és az összes fúziós neutron elegendő energiával rendelkezik az U-238 hasadásához.
Az U-238 spontán hasadási sebessége 35-ször nagyobb, mint az U-235, 5,51 fiss/s*kg. Emiatt nem lehet ágyúbombákban töltetként/reflektorként használni, mert megfelelő tömege (200-300 kg) túl magas neutron hátteret hoz létre.
A tiszta U-238 fajlagos radioaktivitása 0,333 mikrocurie/g.
Ennek az uránizotópnak egy fontos alkalmazási területe a plutónium-239 előállítása. A plutónium számos reakció során keletkezik, amelyek egy neutron U-238 atom általi befogása után kezdődnek. A 235. izotópban természetes vagy részlegesen dúsított uránt tartalmazó reaktorfűtőanyag bizonyos arányban tartalmaz plutóniumot az üzemanyagciklus végén.
U-233 és U-232.
Ez a 162 000 éves felezési idejű uránizotóp a természetben nem fordul elő. A tórium-232-ből neutronbesugárzással nyerhető, hasonlóan a plutónium előállításához:
Th 232 + n -> Th 233
Th 233 -> (22,2 m, béta bomlás) -> Pa 233
Pa 233 -> (27,0 nap, béta-bomlás) -> U 233
Ezzel együtt egy kétlépcsős mellékreakció léphet fel, amelyet az U-232 képződése koronáz meg:
Th 232 + n -> T 231 + 2n
Th 231 -> (25,5 óra, béta-bomlás) -> Pa 231
Pa 231 + n -> Pa 232
Pa 232 -> (1,31 nap, béta-bomlás) -> U 232
A reakció során az urán-232 termelése nagymértékben függ a gyors (nem termikus) neutronok jelenlététől, mivel e ciklus első reakciójának keresztmetszete túl kicsi a termikus sebességekhez. Ha a kiindulási anyagban Th-230 van, akkor az U-232 képződését a következő reakció egészíti ki:
Th 230 + n -> Th 231
és így tovább, mint fent.
Az U-232 jelenléte nagyon fontos a bomlási sorrend miatt:
U 232 -> (76 év, alfa-bomlás) -> Th 228
Th 228 -> (1,913 év, alfa-bomlás) -> Ra 224
Ra 224 -> (3,64 nap, alfa- és gamma-bomlás) -> Rn 220
Rn 220 -> (55,6 s, alfa-bomlás) -> Po 216
Po 216 -> (0,155 s, alfa-bomlás) -> Pb 212
P -212 -> (10,64 óra, béta- és gamma-bomlás) -> Bi 212
Bi 212 -> (60,6 perc, béta- és gamma-bomlás) -> Po 212
alfa- és gamma-bomlás) -> Tl 208
Po 212 -> (3x10 -7 s, alfa-bomlás) -> Pb 208 (stabil)
Tl 208 -> (3,06 perc, béta- és gamma-bomlás) -> Pb 208
A Ra-224 gyors bomlási sorozatának kezdetekor nagyszámú energetikai gamma-sugarat bocsátanak ki. A teljes energia mintegy 85%-a a sorozat utolsó tagjának, a tantál-208-nak a bomlása során keletkezik, a gamma-sugarak energiája eléri a 2,6 MeV-ot.
Az U-232 felhalmozódása elkerülhetetlen az U-233 gyártása során. Ez hasonló a Pu-239 mellett más plutónium izotópok felhalmozódásához, csak jóval kisebb mértékben. A ciklus első reakciójához legalább 6 MeV energiájú neutronokra van szükség. Nagyon kis számú hasadási neutron rendelkezik ilyen energiával, és ha a tóriumtenyésztő zóna a reaktor olyan részében található, ahol közepesen gyors neutronokkal (~ 500 keV) van besugározva, akkor ez a reakció gyakorlatilag kizárható. A második reakció (Th-230-zal) kiválóan megy a termikus neutronokkal is. Ezért az U-232 képződésének csökkenése megköveteli a tórium feltöltését minimális Th-230 koncentrációval.
A fenti óvintézkedések 5 ppm (0,0005%) U-232 U-233-tartalomhoz vezetnek.
A kereskedelmi nukleáris üzemanyagciklusban az U-232 készletezése nem túl nagy hátrány, sőt kívánatos, mivel csökkenti az urán fegyverkezési célú elterjedésének lehetőségét. Az üzemanyag-megtakarítás érdekében feldolgozása és újrafelhasználása után az U-232 szintje eléri a 0,1-0,2% -ot. A speciálisan kialakított rendszerekben ez az izotóp 0,5-1%-os koncentrációban halmozódik fel.
Az U-232-t tartalmazó U-233 előállítása utáni első néhány évben a Th-228 állandó szinten marad, egyensúlyban van saját bomlásával. Ebben az időszakban a gamma-sugárzás háttérértéke kialakul és stabilizálódik. Így az első néhány évben az előállított U-233 tömege jelentős gamma-sugárzást bocsáthat ki. Egy tíz kilogrammos gömb fegyverminőségű U-233 (5 ppm U-232) 11 mr/h hátteret hoz létre 1 m-en 1 hónappal a gyártás után, 110 mr/h egy év után, 200 mr/h 2 év után. . A bombamagok összeszerelésére használt hagyományos kesztyűtartó gyorsan biztonsági problémákat okoz az alkalmazottak számára. Az 5 rem éves dózishatárt már csak 25 óra ilyen anyaggal végzett munka után lépjük túl. Még a friss U-233 (a gyártástól számított 1 hónap) is heti tíz órára korlátozza az összeszerelési időt.
Egy teljesen összeszerelt fegyverben a sugárzás szintje csökkenthető a töltés test általi elnyelésével. A modern, könnyű eszközökben a csökkentés nem haladja meg a 10-szeresét, ami biztonsági problémákat okoz. Nehezebb töltéseknél az elnyelés sokkal erősebb - 100-1000-szeres. A berillium reflektor növeli a neutron háttér szintjét:
Legyen 9 + gamma kvantum -> Be 8 + neutron
Az U-232 gamma-sugarak jellegzetes jelzést alkotnak, és érzékelhetők és nyomon követhetők a mozgás és az atomi töltés jelenléte szempontjából.
A tóriumciklus során előállított, speciálisan denaturált U-233 (0,5-1,0% U-232) még nagyobb veszélyt jelent. Ugyanaz a fent leírt 10 kilogrammos gömb, csak ilyen anyagból, 1 m távolságban 1 hónap után 11 rem/óra, év múlva 110 rem/óra, 2 év után 200 rem/óra hátteret hoz létre. Az ilyen urán feldolgozása és előállítása csak speciális dobozokban, mechanikus manipulátorok segítségével történik (ezeket atomerőművek üzemanyag-kazettáinak létrehozására használják). Ha megpróbál atombombát készíteni ebből az anyagból, még a sugárzás 1000-szeres csökkentésével is, az ilyen termékkel való közvetlen érintkezés évente 25 órára korlátozódik. Így az U-232 jelentős hányadának jelenléte a hasadóanyagban rendkívül kényelmetlenné teszi a katonai felhasználást.
Az U-232 rövid felezési ideje az alfa-részecskék nagyon aktív forrásává teszi. Az 1% U-232-t tartalmazó U-233 háromszor alfa-radioaktívabb, mint a fegyveres minőségű plutónium, ezért radiotoxikusabb. Ez az alfa-aktivitás neutronok keletkezését okozza a könnyű töltéselemekben, ami még komolyabb problémát jelent, mint a berillium reakciója a gamma-kvantumokkal. A probléma minimalizálása érdekében az olyan elemek jelenlétét, mint a berillium, bór, fluor, lítium, a lehető legalacsonyabbnak kell lennie. A neutronháttér jelenléte egyáltalán nem befolyásolja az implóziós rendszereket, mivel ez még mindig kisebb, mint a plutóniumé. Az ágyúprojekteknél a könnyű anyagoknál egy rész a millióhoz az előírt tisztasági szint. Bár az urán ilyen jellegű tisztítása nem triviális feladat, nem esik túl a szokásos kémiai tisztítási módszerek keretein. Ezt bizonyítja legalábbis, hogy az elektronikai ipar képes még nagyobb tisztaságú szilíciumot gyártani.
Az U-233 spontán hasadási sebessége 0,47 hasadás/s*kg. Az U-233 spontán hasadási sebessége 720 hasadás/s*kg. Az U-233 fajlagos radioaktivitása 9,636 millicurie/g, ami a plutónium alfa-aktivitása (és radiotoxicitása) körülbelül 15%-a. Mindössze 1% U-232 növeli a radioaktivitást 212 millicurie/g-ra.
Az erős gamma és neutron radioaktivitás hátránya ellenére az U-233 kiváló hasadóanyag az atombomba magjához. Kritikus tömege kisebb, mint az U-235, és a plutóniumhoz hasonló nukleáris jellemzőkkel rendelkezik. Az Egyesült Államok az 1957-es Teáskanna hadműveletben tesztelte az U-233 alapú tölteteket. India nagy jelentőséget tulajdonít az U-233-nak a fegyverkutatás és -gyártás részeként, és hivatalosan is bevonta az izotóp előállítását nukleáris programjába.
kimerült uránium.
Az U-235 természetes uránból való kinyerése után a megmaradt anyagot „szegényített uránnak” nevezik, mert. a 235. izotópban kimerült. Az Egyesült Államok körülbelül 560 000 tonna szegényített urán-hexafluoridot (UF 6 ) tárol az Egyesült Államok Energiaügyi Minisztériumának három gázdiffúziós dúsító létesítményében: Paducah, Kentucky; az Ohio állambeli Portsmouthban; és a Tennessee állambeli Oak Ridge-ben.
A szegényített urán fele olyan radioaktív, mint a természetes urán, elsősorban az U-234 eltávolítása miatt. Mivel az urán fő felhasználása az energiatermelés, a szegényített urán haszontalan, csekély gazdasági értékű termék. A szegényített urán felhasználásának módjainak megtalálása nagy kihívás a dúsító cégek számára.
Használata alapvetően az urán nagy sűrűségével és viszonylag alacsony költségével függ össze. A szegényített urán két legfontosabb felhasználási módja a sugárzás elleni védelem (furcsa módon) és ballasztként repülési alkalmazásokban, például repülőgép-vezérlőfelületeken. Minden Boeing 747 1500 kg szegényített uránt tartalmaz erre a célra. A szegényített uránt nagyrészt olajkútfúrásokban használják ütőrudak formájában (huzalos fúrásnál), súlya a szerszámot fúrófolyadékkal töltött kutakba süllyeszti. Ezt az anyagot nagy sebességű giroszkóp rotorokban, nagy lendkerekekben is használják, ballasztként űrhajókban és versenyjachtokban.
De az urán legismertebb felhasználása az amerikai páncéltörő lövedékek magja. Egy bizonyos ötvözet más fémekkel és hőkezeléssel (2% Mo-val vagy 0,75% Ti-vel ötvözve, a fém gyors kioltása 850 °C-ra vízben vagy olajban, további 450 °C-on tartva 5 órán keresztül) fémes urán lesz. keményebb és erősebb, mint az acél (szakítószilárdság > 1600 MPa). Nagy sűrűségével kombinálva ez rendkívül hatékonysá teszi az edzett uránt a páncélok áthatolásában, ami hasonló a jóval drágább egykristályos volfrámhoz. A páncél megsemmisítésének folyamatát az urán nagy részének porrá őrlése, a por behatolása a védett objektumba és a levegőben a másik oldalról történő begyulladása kíséri. Körülbelül 300 tonna szegényített urán maradt a csatatéren a Sivatagi Vihar alatt (főleg A-10-es támadórepülőgépek 30 mm-es GAU-8 ágyúinak maradványai, mindegyik lövedék 272 gramm uránötvözetet tartalmazott).
A szegényített uránt a modern harckocsipáncélzatokban használják, például az M-1 Abrams harckocsiban.
Neutronbefogás U-235 és U-238
Urándúsítás
A Manhattan Project során a természetes urán a "tuballoy" (rövidítve "Tu") nevet kapta a projekt "Tube Alloy Division"-ja miatt, ez a név még mindig előfordul a természetes vagy szegényített uránnal kapcsolatban. A nagymértékben dúsított urán (különösen a fegyverdúsítás) kódneve „oralloy” (rövidítve „Oy”). A „Q-metal”, „depletalloy” és „D-38” elnevezések csak a szegényített uránra vonatkoznak.
Gyakorlatilag fontos uránvegyület az urán-hexafluorid UF 6 . Ez az egyetlen stabil és erősen illékony uránvegyület, amelyet izotópjainak - gázdiffúziós és centrifugálási - elválasztásánál használnak. Alkalmazásának ebből a szempontból fontos, hogy a fluornak csak egy izotópja legyen (ez nem okoz további bonyolító tömegkülönbséget), és hogy az UF 6 sztöchiometrikus vegyület (pontosan 6 fluoratomból és 1 uránatomból áll). Szobahőmérsékleten színtelen kristály, és 56 ° C-ra melegítve szublimál (elpárolog anélkül, hogy folyékony fázisba kerülne). Olvadáspontja 64 °C, sűrűsége 4,87 szilárd és 3,86 folyadék. Ez a fluor a legtöbb fémet és oxidot korrodálja, kivéve az alumíniumot (a vékony oxidfilm jelenléte miatt) és a nikkelt (a nikkel-fluorid film képződése miatt). A legtöbb urán-hexafluorid berendezés alumínium vagy nikkelezett.
Egyéb vegyületek közül érdemes megemlíteni az UH 3 urán-hidridet. A Manhattan Project részeként Los Alamosban tanulmányozták atombomba anyagaként. Elméletileg a jelenlévő hidrogénatomoknak olyan sebességre kellene lelassítaniuk a neutronokat, hogy az U-235 atomok általi elnyelésük abszorpciós keresztmetszete sokkal nagyobb legyen. Bár ez kevésbé hatásossá tehette volna a bombát, még maradt remény a szükséges urán tömegének csökkentésére. Már a háború utáni tanulmányok váratlanul alacsony hidridsűrűséget (csak 8) és kis valós befogási keresztmetszetet mutattak ki, ami működésképtelenné tette ezt a sémát. 1953-ban az UH 3 magos robbanóbombák Upshot-Knothole hadműveletében végzett tesztek ezt igazolták, és nagyon kevés popot produkált.
A második világháború előtt az urán ritka fémnek számított. Ma már ismert, hogy az urán gyakoribb, mint a higany vagy az ezüst, és az ipari ércekben körülbelül ugyanolyan koncentrációban található meg, mint az arzén vagy a molibdén. Átlagos koncentrációja a földkéregben körülbelül 2 rész-1 millió, kristályos kőzetek tartalmát tekintve a 48. helyen áll. A litoszférában az urán nagyobb mennyiségben található, mint az olyan olcsó anyagok, mint a cink és a bór, amelyek 4 g/t koncentrációban fordulnak elő. A gránitkőzetek urántartalma elégséges ahhoz, hogy a radon radioaktív gáz, bomlástermék, komoly biológiai veszélyt jelentsen azokon a helyeken, ahol gránit kerül felszínre. A tengervízben is találtak uránt, 150 µg/m 3 koncentrációban.
Az urán elegendő koncentrációban 150 különböző ásványban, kis mennyiségben további 50 ásványban fordul elő. Eredetileg magmás hidrotermikus erekben és pegmatitokban, köztük uraninitben és szurokkeverékben található. Ezek az ércek uránt tartalmaznak dioxid formájában, amelynek átlagos összetétele az oxidáció mértékétől függően UO 2 és UO 2,67 között van. Egyéb gazdasági jelentőségű ércek: autanit, kalcium-hidrát, uranil-foszfát; tobernit, hidratált réz-uranil-foszfát; koffinit, hidratált urán-szilikát; karnotit, kálium-hidrát uranil-vanadát. Az uránércek az egész világon megtalálhatók. A készleteket és a kereskedelmi ügyleteket U 3 O 8 egyenértéktömegben fejezik ki. Egy kilogramm U 3 O 8 átlagosan körülbelül 40 dollárba kerül.
A gyantakeverék, a leggazdagabb uránérc lelőhelyei főleg Kanadában, Kongóban és az USA-ban találhatók. Az Egyesült Államokban bányászott urán nagy részét Utah, Colorado, New Mexico, Arizona és Wyoming államokban nyert karnotitból állítják elő. Az 1955-ben Coloradóban felfedezett koffinit nevű ásvány igen gazdag érc – urántartalma ~61%. Ezt követően koffinitot találtak Wyomingban és Arizonában. 1990-ben az Egyesült Államokban 3417 tonnát állítottak elő uránkoncentrátumot.
Az uránércek általában kis mennyiségben tartalmazzák az urántartalmú ásványt, ezért előzetes kitermelésre és dúsításra van szükség. A fizikai elválasztás (gravitáció, flotáció, elektrosztatika) az uránra nem alkalmazható, hidrometallurgiai módszerekről van szó - az ércfeldolgozás szokásos első lépése a kilúgozás.
A klasszikus savas kilúgozási eljárás során az ércet először aprítják és pörkölik a dehidratáláshoz, a széntartalmú frakciókat eltávolítják, szulfatizálják, és oxidálják a kioldódást akadályozó redukálószereket. Az elegyet ezután kénsavval és salétromsavval kezeljük. Az urán urán szurokcsapadékban szulfátok formájában uranil-szulfáttá, rádiumba és más fémekké alakul át. Marónátron hozzáadásával az urán kicsapódik nátrium-diuránát Na 2 U 2 O 7 .6H 2 O formájában.
Az urán ércből történő kinyerésének klasszikus módszereit ma már olyan eljárások egészítik ki, mint az oldószeres extrakció, ioncsere és bepárlás.
Az oldószeres extrakció során az uránércet eltávolítják a savanyított kőzetlúgból oldószerek keverékével, például tributil-foszfáttal kerozinban. A modern ipari eljárásokban oldószerként alkil-foszforsavak (pl. di(2-etilhexil)-foszforsav) és szekunder és tercier alkil-aminok jelennek meg.
Általános szabály, hogy az oldószeres extrakciót előnyben részesítik az ioncserélő módszerekkel szemben, ha az oldat urántartalma a savas kilúgozás után meghaladja az 1 grammot literenként. Nem alkalmazható azonban az urán karbonátoldatokból történő redukálására.
A fegyvertisztaságú uránt általában nátrium-diuránátból nyerik, további tisztítással, tributil-foszfátos finomítási eljárással. Kezdetben Na 2 U 2 O 7 .6H 2 O-t oldanak fel salétromsavban a nyers oldat elkészítéséhez. Az uránt szelektíven távolítják el belőle úgy, hogy az oldatot tributil-foszfáttal kerozinnal vagy más megfelelő szénhidrogén keverékkel hígítják. Végül az urán a tributil-foszfátból savanyított vízbe kerül, hogy elkülönítse a nagy tisztaságú uranil-nitrátot. A nitrátot UO 3 -dá kalcinálják, amely hidrogénatmoszférában UO 2 -dá redukálódik. Az UO 2 vízmentes hidrogén-fluoridban (HF) UF 4 -dá alakul.
Az urán fémet az uránhalogenidek (általában urán-tetrafluorid) magnéziummal történő redukálásával állítják elő exoterm reakció során egy "bombában" - egy zárt tartályban, általában acélban, ez az elterjedt technika a "termit eljárás". Az urán fém előállítását a magnézium-tetrafluorid redukciójával néha Ames-eljárásnak is nevezik, az Ames-i Iowai Egyetem után, ahol F. H. Spedding kémikus és csoportja 1942-ben fejlesztette ki az eljárást.
A "bombában" a reakciók 1300 °C feletti hőmérsékleten mennek végbe. Erős acéltok szükséges, hogy ellenálljon a benne lévő nagy nyomásnak. A "bombát" UF 4 granulátummal töltik fel, és feleslegben finoman diszpergált magnéziummal borítják, és 500-700 °C-ra melegítik, ettől a pillanattól kezdve önmelegedési reakció indul meg. A reakcióhő elegendő ahhoz, hogy a fémuránból és salak-magnézium-fluorid MF 2-ből álló "bomba" töltetét megolvasztja. Ugyanez a salak elválik és felúszik. A „bombát” lehűtve egy fémurán tuskó keletkezik, amely hidrogéntartalma ellenére a kereskedelemben kapható legjobb minőségű, és jól használható atomerőművi fűtőanyagként.
A fémet úgy is nyerik, hogy az urán-oxidokat kalciummal, alumíniummal vagy szénnel magas hőmérsékleten redukálják; vagy a CaCl 2 és NaCl olvadékban oldott KUF 5 vagy UF 4 elektrolízisével. A nagy tisztaságú uránt vékony filamentum felületén uránhalogenidek hőbontásával lehet előállítani.
Az urándúsítási folyamat végén általában 0,25-0,4% U-235 marad a hulladékban, mivel ennek az izotópnak a végső kinyerése gazdaságilag nem kifizetődő (olcsóbb több nyersanyag vásárlása). Az USA-ban a nyersanyagok U-235 maradéktartalma a gyártás után az 1963-as 0,2531%-ról a 70-es évekre 0,30%-ra nőtt a természetes urán költségének csökkenése miatt.
A koncentrátor elválasztási teljesítményét a feldolgozott anyag tömegében (MPM) mérik időegységenként, például MPP-kg/év vagy MPP-tonna/év. Egy adott kapacitású vállalkozás dúsított termékének kibocsátása a bemeneti kőzetben, a kibocsátott hulladékban és a végtermékben a kívánt izotóp koncentrációjától is függ. Egy hasznos izotóp kezdeti tartalmát általában a természetes tartalma határozza meg. De a másik két paraméter változhat. Ha az izotóp kivonási fokát a kiindulási anyagból csökkentjük, akkor növelhető a felszabadulás sebessége, de ennek ára a szükséges nyersanyagtömeg növekedése lesz. Ez a relációtól függ:
ahol P a termék hozama, U az elválasztóképesség, N P , N F , N W az izotóp moláris koncentrációi a végtermékben, a nyersanyagokban és a hulladékban. V(N P), V(N W), V(N F) elválasztási potenciál függvények minden koncentrációhoz. Meghatározásuk a következő:
![]()
0,25%-os maradék koncentrációt feltételezve egy 3100 MPP-kg/év üzem évi 15 kg 90%-os U-235-öt termelne természetes uránból. Ha nyersanyagként 3% U-235-öt (atomerőművek tüzelőanyaga) és 0,7% koncentrációt veszünk a termelési hulladékban, akkor 886 MPP-kg/év kapacitás elegendő ugyanerre a teljesítményre.
Elválasztási módszerek. A következő technológiákat használták az urán elválasztására egykor vagy úgy:
További figyelmet kell fordítani a következő, iparilag még nem használt módszerekre:
Ezeket a módszereket részletesen az "Izotópszétválasztás módszerei" című cikk tárgyalja, itt az uránnal kapcsolatos megjegyzéseket adjuk meg.
Elektromágneses elválasztás.
Történelmileg ez volt az első technika, amely képes volt fegyverminőségű urán előállítására. A második világháború alatt az Oak Ridge-i Y-12 elektromágneses szeparátorban használták. Két elválasztási fokozat elegendő az urán 80-90%-os dúsításához. Az akkoriban rendelkezésre álló másik két módszer - gázdiffúzió, folyékony termikus diffúzió - az urán kezdeti dúsítására, illetve az elektromágneses szeparátor hozamának növelésére szolgált a természetes urán alapanyaghoz viszonyítva. A hirosimai bombában használt összes uránt ezzel a technológiával állították elő.
A magas rezsiköltségek miatt az Y-12-t 1946-ban bezárták. Újabban csak Irak próbálta iparosítani ezt a módszert nukleáris programjában.
Gáz diffúzió.
Az első technológia, amelyet gyakorlatilag ipari méretekben alkalmaznak. Annak ellenére, hogy több ezer fokozatot igényel a nagymértékű dúsítás, ez költséghatékonyabb módszer, mint az elektromágneses elválasztás. Az U-235 dúsító gázdiffúziós berendezések hatalmasak és nagy termelési kapacitással rendelkeznek.
A fő nehézséget a megbízható gázdiffúziós gátak létrehozása jelenti, amelyek képesek ellenállni az UF 6 korrozív hatásának. Az ilyen korlátoknak két fő típusa van: vékony porózus membránok és egyedi csövekből összeállított korlátok. A membránok maratással kialakított pórusokkal rendelkező filmek. Például a salétromsav pácolja a 40/60 Au/Ag (Ag/Zn) ötvözetet; vagy alufólia elektrolitikus maratásával törékeny alumínium membránt kaphatunk. A kompozit korlátokat kis, különálló elemekből állítják össze, amelyek egy viszonylag vastag porózus terelőlemezbe vannak csomagolva.
A diffúziós akadályok gyártásának technológiája továbbra is besorolás alatt áll minden olyan országban, ahol kifejlesztették.
A második világháború alatt épült K-25 Oak Ridge-i létesítmény 3024 dúsítási szakaszból állt, és az 1970-es évek végéig működött. A megfelelő záróanyag kifejlesztése nehéznek bizonyult, ami némi késést okozott az üzem háború utáni üzembe helyezésében, bár még egy részben elkészült üzem is hozzájárult a Little Boy U-235-ös felhalmozásához. Míg a gátakat szinterezett nikkelporból készítettek, az elektrolitikusan maratott alumíniumból ígéretes membránok létrehozására tett kísérletek kudarcot vallottak. A K-25 eredetileg 162 000 m2 membránfelületet tartalmazott. Ez a létesítmény – bővítéssel – a hatvanas években az Egyesült Államok hadseregének szánt uránium nagy részét állította elő. A gázdiffúziós akadályok fejlesztésével az üzem termelékenysége 23-szorosára nőtt.
A diffúziós termelés az elektromágneseshez képest sokkal kevesebb villamos energiát fogyaszt, de a fogyasztása még így is elég nagy. 1981-ben a korszerűsítés után fajlagos teljesítményfelvétele 2370 kWh/MPP-kg volt.
Míg az alacsony dúsítású urán értékes nyersanyag a nagymértékben dúsított urán előállításához, az alacsony dúsítású gáznemű diffúziós üzemeket nem lehet könnyen átalakítani nagy dúsítású urán előállítására. A nagymértékű dúsítás sok kisebb szakaszt igényel a dúsítási tényező meredek csökkenése és a kritikussági problémák (az urán kritikus tömegének felhalmozódása) miatt a nagyobb blokkokban.
A dúsítórendszer hatalmas mérete miatt hosszú ideig kell feltölteni anyaggal (dúsított anyaggal), mielőtt a termék kilép. Általában ez az egyensúlyi idő 1-3 hónap.
A gázdiffúziós technológiát számos országban széles körben alkalmazzák, még Argentína is létrehozott egy működő dúsító üzemet titkos fegyverprogramjához (jelenleg megszűnt). 1979-ben az összes urán több mint 98%-át ezzel az eljárással állították elő. Az 1980-as évek közepére ez az arány a centrifugálási módszer bevezetésével 95%-ra csökkent.
Folyékony termikus diffúzió.
A folyékony termikus diffúzió volt az első technológia, amely jelentős mennyiségű alacsony dúsítású uránt állított elő. Az USA-ban a Manhattan Project során használták az Y-12 szeparátor hatékonyságának növelésére. Ez a legegyszerűbb az összes elválasztási módszer közül, de az U-235 dúsítási határértéke csak ~1% (az Oak Ridge-i S-50 üzem 0,85-0,89% urán-235-öt termelt a végtermékben). Ezenkívül a hődiffúzió hatalmas hőmennyiséget igényel.
Gázcentrifugálás.
Az izotópleválasztás domináns módszere az új iparágakban, bár a meglévő létesítmények többnyire gázdiffúziós. Mindegyik centrifuga sokkal nagyobb elválasztási tényezőt biztosít, mint egy gázfokozat. Sokkal kevesebb fokozatra van szükség, csak körülbelül ezerre, bár minden centrifuga költsége sokkal magasabb.
A gázcentrifugálás a gázdiffúzióhoz szükséges energia ~1/10-ét igényli (energiafogyasztása 100-250 kWh/MPH-kg), és lehetővé teszi a könnyebb skálázást.
A fejlődő nukleáris országok közül ez a meglehetősen kifinomult technológia Pakisztán és India tulajdonában van.
Aerodinamikai elválasztás.
Az aerodinamikus elválasztást Dél-Afrikában (UCOR eljárás vortex csövekkel 6 bar nyomáson) és Németországban (0,25-0,5 bar nyomáson működő íves fúvókákkal) fejlesztették ki.
Ezt a módszert egyedül Dél-Afrika alkalmazta, ahol a nyolcvanas évek végén bezárt valindabai üzemben 400 kg fegyveres minőségű uránt állítottak elő. Elválasztási tényező ~1,015, energiafogyasztás ~3300 kWh/MPP-kg.
Párolgás lézerrel.
AVLIS (atomi gőzlézeres izotóp szétválasztás). A technológia soha nem került gyártásba, az 1970-es és 80-as években az USA-ban fejlesztették ki. és kihalt az elválasztó kapacitások általános feleslege és az arzenál csökkenése miatt.
Kémiai elválasztás.
Az urán kémiai szétválasztását Japánban és Franciaországban fejlesztették ki, de az AVLIS-hez hasonlóan soha nem használták. A francia Chemex-módszer ellenáramlást alkalmaz két egymással nem elegyedő folyadékból álló magas oszlopban, amelyek mindegyike oldott uránt tartalmaz. A japán Asahi módszer cserereakciót alkalmaz egy vizes oldat és egy finomra őrölt gyanta között, amelyen az oldat lassan átszivárog. Mindkét módszerhez katalizátorra van szükség a koncentrálási folyamat felgyorsításához. A Chemex eljárás 600 kWh/MPP-kg villamos energiát igényel.
Irak ezt a technológiát (Chemex/Asahi vegyes gyártás formájában) fejlesztette ki az U-235 dúsítására 6-8%-ig, majd ezt követően a calutronban.
Ezen módszerek hozzávetőleges energiahatékonysága a gáz diffúzióval kapcsolatban:
kevesebb, mint 0,01? AVLIS (ha ipari felhasználásra kerül)
0,10-0,04 gázcentrifugálás
0,30 kémiai elválasztás
1.00 gázdiffúzió
1.50 aerodinamikai elválasztás
magas elektromágneses elválasztás
magas folyadék termikus diffúzió
A 6.0 Nukleáris fegyverek GYIK fordítása, Carey Sublette, . Fap suite nero. Kerámia csempe fap luce. . Nagy acélgolyók. Jó acélgolyók.
Hasadási szilánkok
A hasadás jellegzetes vonása, hogy a hasadás eredményeként keletkezett töredékek tömege általában jelentősen eltérő. A legvalószínűbb, 235 U-os hasadás esetén a töredék tömegaránya 1,46. Ebben az esetben egy nehéz töredék tömegszáma 139, a könnyűé - 95. Nem az egyetlen lehetséges ilyen tömegű töredékre osztani. A 235 U méretű hasadási töredékek termikus neutronok szerinti tömegeloszlását a ábra mutatja. 8. A hasadási termékek között A = 72-161 és Z = 30-65 értékű töredékeket találtunk. A két egyenlő tömegű töredékre való hasadás valószínűsége nem egyenlő nullával. Termikus neutronos hasadás esetén a szimmetrikus hasadás valószínűsége hozzávetőleg három nagyságrenddel kisebb, mint a legvalószínűbb A = 139 és 95 darabokra való hasadás esetén. A cseppmodell azonban nem zárja ki az aszimmetrikus hasadás lehetőségét. még csak minőségileg sem magyarázza meg az ilyen hasadás fő szabályszerűségeit. Az aszimmetrikus hasadás a mag héjszerkezetének hatására magyarázható. A sejtmag hajlamos oly módon hasadni, hogy a töredék nukleonjainak nagy része stabil mágikus magot alkot.
A hasadás során az energia nagy része a hasadási fragmentumok mozgási energiája formájában szabadul fel. Ilyen következtetést vonhatunk le abból, hogy két érintkező fragmentum Coulomb-energiája megközelítőleg megegyezik a hasadási energiával. Az elektromos taszító erők hatására a töredékek Coulomb-energiája mozgási energiává alakul.
A töredékek E kinetikus energiái és M tömegei között a következő összefüggés áll fenn, ami az impulzusmegmaradás törvényéből következik:
ahol E l és M l és könnyű töredékre, E t és M t pedig nehéz töredékre utal. Ezt az összefüggést felhasználva a töredékek energiaeloszlásából megkaphatjuk a töredékek tömegeloszlását (9. ábra). Az energiaeloszlási paramétereket, valamint néhány egyéb jellemzőt a 235 U méretű, termikus neutronokkal történő hasadásról a táblázat tartalmazza. egy.
1. táblázat Könnyű és nehéz töredékek jellemzői a 235 U termikus neutronok általi legvalószínűbb hasadásához
Jellegzetes |
Light Shard |
Nehéz szilánk |
| A tömegszám | ||
| Elektromos töltés Z | ||
| Kinetikus energia E, MeV | ||
| Futásteljesítmény levegőben normál körülmények között, mm |
A hasadási töredékek kinetikai energiája viszonylag kevéssé függ a hasadó mag gerjesztési energiájától, mivel a többletenergiát általában a töredékek belső állapotának gerjesztésére használják fel.
A 10. ábra a 234 U méretű és nehezebb magok hasadási töredékeinek tömegeloszlását mutatja. Látható, hogy a nehéz fragmentumok tömegeloszlása közeli, míg a könnyű töredékek átlagos tömege ~90-től 234 U-nál ~114-ig 256 Fm-ig változik. Ez különösen jól látszik a 11. ábrán.
A könnyű csoport átlagos tömege csaknem lineárisan növekszik a hasadó mag tömegével, míg a nehéz csoport átlagos tömege gyakorlatilag változatlan marad (A140). Így gyakorlatilag minden további nukleon könnyű töredékekké megy. A 10. ábrán az atommagok varázslatos számú proton- és neutronterülete árnyékolt. Z = 50 esetén a stabil magok Z/A 0,4-nek felelnek meg (A = 125). A neutronban gazdag hasadási töredékek Z/A-értéke ~0,38-ig (A = 132), i.e. kb 7 "extra" neutron. A töredékek nehéz csoportjának szélén található a kétszeresen mágikus 132 Sn mag (Z = 50, N = 82). Ez a rendkívül stabil konfiguráció határozza meg a nehéz fragmentumok tömegeloszlásának alsó végét. A könnyű töredékek esetében ez a hatás nem létezik. A fénytöredékek tömegeloszlása gyakorlatilag nem esik az N = 50 mágikus szám tartományába, és sokkal kevésbé határozzák meg a héjhatások. A nehéz fragmentum képződése után "maradt" nukleonokból jön létre.